Los biofertilizantes líquidos enriquecidos con rizobacterias han demostrado que mejoran la calidad de los cultivos y estimulan el desarrollo de su sistema radicular y foliar. En esta investigación se buscó evaluar el efecto de biol combinado con Azospirillum brasilense en plántulas de Zea Mays, para esto se ejecutó la etapa exploratoria en la que se utilizó un diseño factorial 31 al azar donde se usaron 3 fertilizantes: el Azospirillum brasilense solo, el biol solo y la combinación del Azospirillumbrasilense con el biol y como control no se utilizó fertilizante.
Resumen
Los ensayos se hicieron en macetas con capacidad de un 1 kg de suelo, durante 8 semanas se evaluaron parámetros biométricos donde se evidencio cambios en la biomasa aérea, entre ellos parámetros importantes como la altura y número de hojas; arrojando resultados poco favorables, por lo cual se empieza una etapa de ajustes, en la que se realiza un cambio de biol y se ejecutó por medio de camas con una capacidad de 1 m3 de suelo y en cada una se sembraron 10 plántulas aplicando los mismos fertilizantes y a su vez se evaluaron los mismos parámetros biométricos durante 14 semanas.
Introducción
La Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO) estima que la demanda de cultivos agrícolas aumentará un 60% para el año 2030 (Allouzi et al., 2022a). Este incremento podría intensificar el uso de fertilizantes químicos y, con ello, generar impactos ambientales importantes (Makádi et al., 2016). Entre estos efectos se encuentran: la pérdida de capacidad del suelo para retener agua, la disminución de nutrientes, una mayor compactación, acidificación y alteraciones en las comunidades bacterianas. Esta última puede reducir grupos clave como Chitinophagaceae y Nitrospiraceae, esenciales en la degradación de polisacáridos (P) y el ciclo del nitrógeno (N) (Chen et al., 2019). Además, el exceso de fertilizantes contribuye a la contaminación de cuerpos de agua por lixiviación y a la emisión de gases de efecto invernadero (Atieno et al., 2020).
En el caso de Estados Unidos, por ejemplo, en 2018 se aplicaron 10,2 millones de toneladas de nitrógeno, un aumento del 2% en la última década, mientras que el uso de fósforo alcanzó 1,1 millones de toneladas (Rai et al., 2023). Estos datos muestran que los fertilizantes NPK siguen siendo productos ampliamente utilizados por su facilidad de aplicación y su larga presencia en el sector agrícola. Sin embargo, sus impactos obligan a buscar alternativas más sostenibles que favorezcan la recuperación del suelo y el fortalecimiento de su microflora (Haiyang Li, 2022).
Leer también: Sostenibilidad sin exclusión: ¿Qué pasa cuando la sostenibilidad no es accesible para todos?
Biofertilizantes
Entre estas alternativas se encuentran los biofertilizantes, los cuales aportan nutrientes a las plantas, mejoran las propiedades del suelo y promueven condiciones microbiológicas más equilibradas y naturales (Chen et al., 2019). Estos insumos también son fundamentales en la agricultura orgánica, ya que permiten mantener una producción eficiente sin comprometer la salud del ambiente ni los principios del desarrollo sostenible (Naciones Unidas, 2015).
Muchos biofertilizantes están compuestos por microorganismos beneficiosos como bacterias y hongos, capaces de establecer relaciones simbióticas con las raíces de las plantas y potenciar su crecimiento. Uno de estos es el biol, un fertilizante líquido que se obtiene mediante la digestión anaerobia (DA) de residuos orgánicos como estiércol o restos alimenticios. Su composición química varía según el material utilizado, especialmente en la relación carbono/nitrógeno (C/N). Debido a su aporte nutricional, el biol se emplea ampliamente como biofertilizante (Sharma et al., 2023).
El proceso de digestión anaerobia se desarrolla en cuatro etapas —hidrólisis, acidogénesis, acetogénesis y metanogénesis— en las que diferentes microorganismos transforman los compuestos orgánicos iniciales (Chin Cheong et al., 2020). Para obtener un biol de calidad, se controla la carga semanal de residuos en el reactor, la producción de biogás, la concentración de metano y los procesos posteriores de higienización o estabilización (Chuda & Ziemiński, 2023). En algunos casos, especialmente con bioles de origen animal, se utilizan técnicas complementarias como centrifugación, coagulación o filtración por membranas de fibras huecas para eliminar impurezas antes de su aplicación agrícola. Sin embargo, prácticas más accesibles, como la inyección de aire para detener la actividad anaerobia, también han mostrado resultados positivos en contextos rurales (Cheong et al., 2020).
Rizobacteria Azospirillum brasilense
Otro microorganismo fundamental en la agricultura sostenible es la rizobacteria Azospirillum brasilense, conocida por su capacidad de fijar nitrógeno atmosférico en asociación con las raíces. Su uso puede mejorar el crecimiento vegetal, aumentar la productividad y fortalecer la competitividad agrícola (Levin et al., 2021). Por ello, la combinación de biol con Azospirillum brasilense representa una fuente conjunta de nutrientes y microorganismos benéficos que promueve el desarrollo vegetal y contribuye al cumplimiento de los Objetivos de Desarrollo Sostenible, especialmente el ODS 2 (Hambre Cero) (Naciones Unidas, 2015).
Diversos estudios respaldan la eficacia de estos bioinsumos. Ramírez (2023) evaluó rizobacterias como Atlantibacter sp. en plántulas de tomatillo, demostrando su capacidad para solubilizar fosfato y favorecer el crecimiento vegetal. Otros trabajos, como los realizados por Hassan y Abbasi en cultivos de trigo, mostraron incrementos significativos en la altura del tallo, crecimiento radicular y acumulación de nutrientes al aplicar mezclas de bacterias como Pseudomonas, Azospirillum y Agrobacterium (Chen et al., 2019).
Leer tambíen: De residuo a recurso: porcinaza como energía y fertilizante sostenible
A partir de esta evidencia, el objetivo de la presente investigación es evaluar los efectos de la biofertilización con bioles enriquecidos con Azospirillum brasilense en suelos deficientes en nutrientes. La finalidad es activar los procesos microbianos del suelo y potenciar el crecimiento de las plantas, promoviendo el uso de bioinsumos como una alternativa viable en sistemas agrícolas sostenibles.
Desarrollo
Materiales y métodos para evaluar los efectos de los biofertilizantes
La muestra de suelo se recolectó en el corregimiento El Hatillo, municipio de Barbosa (Antioquia, Colombia), ubicado en las coordenadas 6°25’11” N y 75°23’33” W, a una altitud de 1.357 m s. n. m. El área de muestreo se seleccionó aleatoriamente y se tomó una muestra a 20 cm de profundidad. Posteriormente, el suelo se secó a temperatura ambiente durante 10 días y se tamizó con malla de 2 mm, siguiendo el protocolo de toma de muestras para análisis de fertilidad del laboratorio BioFertilizar (Osorio, s.f.).
Se realizó un análisis fisicoquímico del suelo, evaluando parámetros como textura, pH, conductividad eléctrica, materia orgánica (MO), fósforo disponible (P-Bray II y P soluble), azufre (S), aluminio intercambiable (cuando pH < 5.5), acidez intercambiable, Ca, Mg, K, Na, capacidad de intercambio catiónico (CIC), Fe, Mn, Cu, Zn, B, N-NO₃ y N-NH₄. También se determinaron relaciones y saturaciones de cationes. De acuerdo con estos resultados, el suelo se clasificó como franco arcillo-arenoso, conforme al método estandarizado del CIAT (CGIAR, s.f.).
Para el ensayo se utilizaron plántulas de maíz de 10 cm de altura inicial. Se sembraron tres plántulas por matera en un total de 12 contenedores, cada uno con 1 kg de suelo. A los 15 días se realizó un raleo para dejar una plántula por matera. Los ensayos se llevaron a cabo en el mismo corregimiento El Hatillo.
Uno de los tratamientos consistió en aplicar biol obtenido de un sistema de digestión anaerobia que procesa residuos animales, especialmente estiércol porcino, con una capacidad de tratamiento de 30 kg/día. Este sistema produce en promedio 65 L de biol por día con una proporción de 1:5 (1 kg de estiércol por 5 L de agua). El biol fue sometido a procesos de higienización, estabilización y caracterización, además de una aireación mediante inyección de oxígeno para detener la actividad microbiana anaerobia y eliminar posibles patógenos.
El segundo tratamiento empleó el microorganismo Azospirillum brasilense, comercialmente conocido como DIMAZOS (Biocultivos), en una concentración de 1 × 10⁸ UFC/ml (Comercial Proveedor et al., 2019).
El diseño experimental incluyó tres tratamientos y un control:
- TA: Azospirillum brasilense
- TB: Biol
- TBA: Biol + Azospirillum brasilense
- C: Control (solo agua)
En el tratamiento TA se aplicaron 5 ml del inoculante por matera al momento de la siembra. En el tratamiento TB se aplicaron 50 ml de biol por matera. Para el tratamiento TBA se aplicaron 5 ml de Azospirillum al inicio más 50 ml de biol de manera semanal. Durante el riego —realizado desde la parte superior de la matera— se aplicaron 50 ml de agua cada 8 días para mantener la proporción del biol.
Después de 90 días de crecimiento, se evaluaron variables biométricas como altura (cm), diámetro del tallo (mm) y número de hojas. Luego se recolectaron las plantas, separando la biomasa foliar y radicular, las cuales fueron pesadas en una balanza analítica para obtener el peso fresco. Posteriormente se secaron en un horno a 60 °C durante 3 días para determinar el peso seco.
Para el análisis foliar, las muestras se enviaron a laboratorio, donde se evaluó el contenido de macro y micronutrientes mediante espectrofotometría de absorción atómica. Para comprobar la colonización de Azospirillum brasilense en la rizósfera, se realizó un cultivo de bacterias oxidantes de amonio (AOB), siguiendo el protocolo del Instituto Geográfico Agustín Codazzi (IGAC).
Resultados y análisis de la etapa exploratoria
Para garantizar que el biol sea un producto estabilizado, de excelente calidad, altamente disponible y asimilable para el adecuado desarrollo de los cultivos y el crecimiento de las plantas de Zea mays, se estableció un proceso de aireación. Este consistió en transferir el biol de un recipiente a otro durante 20 repeticiones, permitiendo que las burbujas generadas en el proceso se disiparon y posteriormente dejando reposar el biol durante 10 minutos antes de aplicarlo a las plántulas. (A.J. Zapata, 2024)
La Tabla 1 presenta los resultados obtenidos de la caracterización del biol estabilizado, derivado de un reactor de fermentación anaerobia de residuos orgánicos para uso agrícola.
Tabla 1. Caracterización del biol
| Parámetro | Unidades | Técnica | Norma | Resultado | NTC 5167/2022 |
| CO | g/l | Titulométrica | 0.99 | >20 | |
| pH (directo) | U pH | Método estándar | NTC 5167 | 7.08 | 2.5–8.5 |
| C.E. (1/100) | dS/m | 0.043 | – | ||
| N-Org. Total | g/l | Titulométrica | NTC 370 | 0.594 | >15 |
| C/N | – | Cálculo matemático | 1.66 | – | |
| Sólidos totales | g/l | Método estándar | NTC 5167 | 10.6 | <40 |
| Sólidos fijos | mg/l | NTC 897 | 4272 | – | |
| Sólidos volátiles | mg/l | Cálculo matemático | 6328 | – | |
| DQO total | mgO₂/l | Método estándar | SM 5220-D | 5450 | – |
La Tabla 1 presenta los resultados de la caracterización del biol, comparados con los valores de referencia de la NTC 5167 de 2022. Estos parámetros permiten entender la calidad del biol y su potencial como biofertilizante.
El pH del biol fue de 7.08, un valor neutro que favorece la disponibilidad de macro y micronutrientes esenciales para el crecimiento de las plantas y para el funcionamiento de procesos metabólicos y estructurales (Zainuddin et al., 2022).
Carbono orgánico
En el caso del carbono orgánico, los resultados están muy por debajo del mínimo exigido por la norma (Icontec, 2022). Esto indica que la mezcla inicial del digestor contenía poca materia orgánica en comparación con la cantidad de agua utilizada. Como consecuencia, el contenido de nitrógeno orgánico total también fue bajo (0.594 g/L), lejos del mínimo normativo de 15 g/L. Esto sugiere que la proporción de dilución fue mayor a la relación 1:5 mencionada previamente. Aunque esto reduce la concentración de nutrientes, el biol siguió siendo adecuado para el ensayo. En estas condiciones, se espera que Azospirillum brasilense contribuya fijando nitrógeno atmosférico y transformándolo en una forma disponible para las plantas (A. J. Zapata, 2024).
Carbono / nitrógeno
Respecto a la relación carbono/nitrógeno (C/N), es importante considerar que durante la digestión anaerobia esta relación disminuye debido al consumo microbiano y a las pérdidas de carbono (como CO y CO₂) y nitrógeno (como amoníaco). Por ello, suele recomendarse iniciar con relaciones C/N superiores, alrededor de 50:1, para finalizar dentro del rango óptimo. En este estudio, los valores finales de C/N fueron inferiores a 30, lo cual se considera adecuado y estable para procesos de fermentación anaerobia (Icontec, 2022).
La conductividad eléctrica registrada fue de 0.043 dS/m. Según Marín García (2003), valores tan bajos pueden deberse al consumo de compuestos solubles durante la fase de crecimiento microbiano. Además, considerando que los suelos salinos presentan conductividades entre 8 y 16 mS/cm, este biol resulta apto para su aplicación en suelos de baja salinidad o en cultivos tolerantes a ella.
Finalmente, el pH neutro del biol es una ventaja agronómica. Biofertilizantes demasiado ácidos o alcalinos pueden alterar el equilibrio del suelo y afectar la disponibilidad de nutrientes. Un pH neutro, en cambio, promueve una absorción eficiente y contribuye a que las plantas crezcan más vigorosas, resistentes y con mejores rendimientos (Marín, 2003).
Tabla 2
La Tabla 2 presenta los resultados de la caracterización del suelo tomado en el distrito El Hatillo, municipio de Barbosa, Antioquia.
Tabla 2. Caracterización del suelo
| Parámetro | Resultado | Unidades | Rango |
| Arena | 50 | % | 20–70 |
| Limo | 20 | % | 30–50 |
| Arcilla | 30 | % | 10–25 |
| Clase | Franco arcilloso arenoso | – | Franco |
| pH | 5.5 | – | 5.5–6.0 |
| C.E. | 0.15 | dS/m | 1–2 |
| M.O. | 5.6 | % | 5–10 |
| P³⁻ | 5 | mg/kg | 15–30 |
| S²⁻ | 47 | mg/kg | 6–12 |
| Al³⁺ | 0 | cmol(+)/kg | <1 |
| Ca²⁺ | 7.2 | cmol(+)/kg | 3–6 |
| Mg²⁺ | 2.2 | cmol(+)/kg | 1.5–2.5 |
| K⁺ | 0.33 | cmol(+)/kg | 0.15–0.30 |
| CEC ef | 9.76 | cmol(+)/kg | 5–10 |
| Fe²⁺ | 53.3 | mg/kg | 25–50 |
| Mn²⁺ | 7.8 | mg/kg | 5–10 |
| Cu | 3.7 | mg/kg | 3–5 |
| Zn | 2.4 | mg/kg | 3–5 |
| B | 0.2 | mg/kg | 0.5–1.0 |
Según la Tabla 2, el suelo corresponde a una textura franco arcillosa arenosa, con pH ligeramente ácido (5.5 unidades). Este resultado indica la ausencia de aluminio intercambiable (Al³⁺), cuya presencia resultaría tóxica para las plantas al impedir el desarrollo completo del sistema radicular, ocupando los sitios efectivos de intercambio del suelo.
Estudios
Estudios realizados en la región del Pacífico Sur de Costa Rica por Montes et al. (Garbanzo-León et al., 2017) indican que los suelos con pH entre 5.5 y 6.7, ligeramente ácidos, suelen tener texturas medias y alta saturación de bases (64–67%). Al comparar estos parámetros con los del suelo de Hatillo, Barbosa, se observa similitud, lo que sugiere bio-disponibilidad de nutrientes necesarios para el crecimiento vegetal.
La capacidad de intercambio catiónico (CIC) mide la habilidad del suelo para adsorber cationes como Ca²⁺, Mg²⁺ y K⁺, y refleja la carga negativa del suelo, determinando los sitios disponibles para retener estos iones (Washington et al., 2014). Según los resultados de la Tabla 2, la CIC es media, suficiente para el desarrollo adecuado de las plantas, y las concentraciones de los cationes son satisfactorias.
La adsorción de aniones puede afectar la nutrición vegetal si los iones como fosfatos o sulfatos no están disponibles. La retención de fosfato por compuestos orgánicos puede originar formas poco solubles (Washington et al., 2014). En este caso, los niveles de P₃⁻ son bajos, indicando deficiencia de fósforo, similar a lo observado en el estudio de Montes, donde se asoció a la presencia de altos niveles residuales de Cu²⁺.
El tallo del maíz es simple, erecto y de gran longitud (hasta 4 m), robusto y sin ramificaciones, similar a la caña. No presenta nudos visibles y su médula esponjosa se aprecia en corte transversal.
Interpretación
La Figura 1 (a) y (b) muestra los resultados de la altura de la planta y el número de hojas obtenidos durante 8 semanas. Los datos indican que la biomasa aérea aumentó más en las plántulas tratadas con Azospirillum + biol, con incrementos de 10 a 20 cm, seguidas por las tratadas solo con biol y luego por Azospirillum brasilense. Esto demuestra que el biol enriquecido con Azospirillum brasilense promovió un desarrollo radicular más rápido, reflejado en el crecimiento aéreo por mayor altura, lo cual influye significativamente en el rendimiento del cultivo, ya que la producción depende de tallos firmes y vigorosos.
Es importante resaltar que tanto el biol como Azospirillum son esenciales: el primero aporta nutrientes escasos en el suelo, mientras que el segundo promueve el crecimiento vegetal mediante fijación de nitrógeno, solubilización de fosfatos y producción de fitohormonas (ácido indolacético, giberelinas y citoquininas), que favorecen la expansión foliar y optimizan el aprovechamiento de recursos (Angulo-Castro et al., 2018).
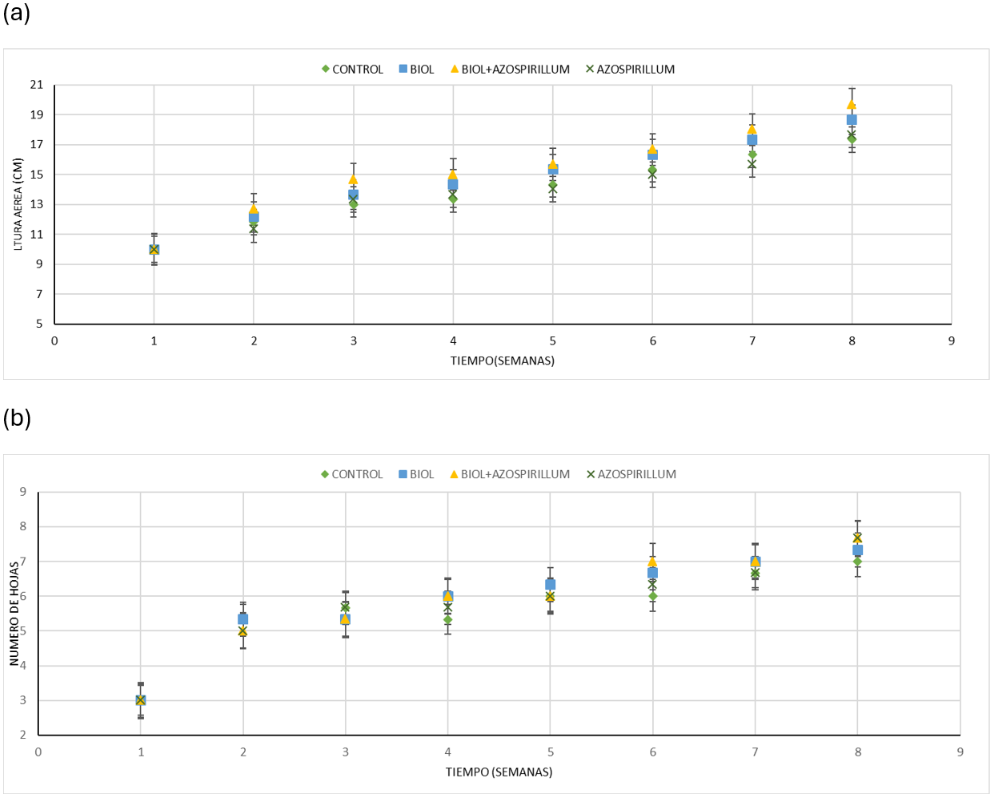
Fig 1. (a) Altura aérea de las plantas de Zea mays en la etapa exploratoria, en relación con el tiempo desde la semana 1 hasta la semana 8. (b) Número de hojas de las plantas de Zea mays en la etapa exploratoria, en relación con el tiempo desde la semana 1 hasta la semana 8. Fuente: (V. Jaramillo & A. Zapata, 2024)
Etapas de crecimiento del maíz
Los investigadores del maíz han desarrollado una guía para identificar las diferentes etapas de crecimiento del maíz. No todas las plantas en el campo alcanzan una etapa determinada al mismo tiempo. Por lo tanto, los investigadores asumen que el cultivo alcanza una etapa específica cuando al menos el 50% de las plantas presentan las características correspondientes. Esto permite a los investigadores referirse a los temas relacionados con etapas de crecimiento específicas y también les posibilita comparar la fenología del maíz bajo diferentes condiciones ambientales y tratamientos experimentales.
Los investigadores dividen las etapas de crecimiento en dos categorías principales: etapas vegetativas (V) y etapas reproductivas (R) (CIBIOGEM, 2003).
Proceso
Las plántulas se plantaron en la etapa V1, donde el collar de la primera hoja era visible. En la etapa V2, el collar de la segunda hoja se volvió visible. Para alcanzar la etapa Vn, la planta debía tener entre 16 y 22 hojas, pero para el momento de la floración, entre 4 y 5 de las hojas inferiores ya se habían perdido. La Figura 1 (b) muestra que las plántulas alcanzaron un máximo de 7 hojas, las cuales son largas, grandes, lanceoladas, alternas y con nervaduras paralelas. También están fuertemente envueltas alrededor del tallo, con vellosidades en la superficie superior, y las puntas de las hojas son muy agudas y cortantes (CIBIOGEM, 2003).
Observación 8 semanas
Después de 8 semanas, las plántulas comenzaron a mostrar un amarillamiento en forma de “V” hacia las puntas de las hojas, como se muestra en la Figura 2. Los síntomas se observaron primero en las hojas más viejas, con las puntas y venas centrales finalmente senescentes. Las hojas con tono verde claro o franjas amarillas pueden indicar deficiencia de potasio. La apariencia amarilla o “quemada” en los bordes de las hojas se desarrolló en necrosis. En las hojas más viejas, las puntas y márgenes finalmente se marchitaron y se tornaron marrones. Las hojas viejas que desarrollaron clorosis internerval pueden mostrar síntomas de deficiencia de magnesio, debido a la baja absorción y translocación de nutrientes por el sistema radicular. Las deficiencias se detectan típicamente entre las etapas de desarrollo V2 y V8 (Instituto de la Potasa y el Fósforo, 2015).
La caracterización del suelo que se muestra en la Tabla 2 indica que el magnesio está presente en concentraciones óptimas (2.2 cmol(+)/kg), al igual que el potasio (0.33 cmol(+)/kg). Sin embargo, según la Figura 3 y el Instituto de la Potasa y el Fósforo (2015), las plantas no pudieron absorber ni translocar los nutrientes desde el sistema radicular hacia el tejido foliar.

Fig 2. (a) Comportamiento de las plántulas de Zea mays en la semana 8. Conjunto de tratamientos que muestran decoloración y quemadura en las hojas. (b) Plántulas de Zea mays en la semana 9, mostrando marchitamiento y etapa de muerte. Fuente: (V. Jaramillo & A. Zapata, 2024)
Evaluación
Después de observar la coloración en las plantas, se evaluó el sistema radicular. La raíz del maíz muestra una estructura compleja en comparación con otras plantas. Para todos los tratamientos en la primera etapa, las raíces se forman endógenamente en el embrión y consisten en la raíz primaria y las raíces escutelares, que aparecen durante la germinación. Las raíces seminales escutelares son una parte importante para la absorción inicial de agua y nutrientes, así como para el establecimiento de la plántula en el suelo.
Las raíces post-embrionarias se forman después de la germinación y continúan creciendo hasta formar un sistema radicular altamente ramificado en plantas adultas. El sistema radicular post-embrionario está compuesto por raíces coronarias o nodales (RC) y raíces aéreas (RA) que aparecen más tarde en los nudos del tallo. Hasta este punto, pueden observarse en la Figura 3, pero no alcanzan las raíces escutelares, y las raíces coronarias —que forman la estructura de anclaje de la raíz— no se formaron adecuadamente debido al área y la cantidad de suelo disponible para cada plántula (CIBIOGEM, 2003).
Observación semana 9
En la novena semana, se observó la muerte de las 12 plántulas. Sus tallos eran débiles y de color marrón, y sus hojas estaban flácidas, con muchas de ellas desprendidas del tallo, como se muestra en la Figura 2 (b).
Las posibles causas de la muerte de las plantas de maíz incluyen factores relacionados con sus condiciones de siembra, como el tipo y la profundidad del suelo. El maíz se adapta bien a todo tipo de suelos, pero los suelos con un pH entre 6 y 7 son los más adecuados. También requiere suelos profundos, ricos en materia orgánica y con buena circulación de drenaje para evitar encharcamientos, los cuales pueden causar asfixia radicular, creando un ambiente anaeróbico en el suelo que conduce a la muerte tanto de plantas como de microorganismos.
Otras posibles razones podrían estar relacionadas con la compra de las plántulas, ya que podrían haber estado previamente afectadas por una enfermedad, o con que el sustrato utilizado contuviera algún microorganismo patógeno que estuviera dañando el sistema radicular de las plantas (Instituto de la Potasa y el Fósforo, 2015).
Metodología etapa de ajuste
Por las razones mencionadas anteriormente, las plantas fueron replantadas, realizando cambios en las condiciones del suelo, biol y área de siembra. La nueva siembra se llevó a cabo en el municipio de Barbosa.
Se utilizaron plántulas de maíz con una longitud inicial de 10 cm. Se sembraron diez plántulas por cama para asegurar un mayor número de réplicas y obtener mejores resultados. Cada cama tenía una capacidad de 1 m³ de suelo.
De acuerdo con el diseño experimental, uno de los tratamientos aplicados fue la adición de biol, obtenido comercialmente teniendo en cuenta su ficha técnica. La decisión de usar un biol comercial se tomó porque, como se mostró en la etapa exploratoria (Tabla 1), los niveles de nutrientes eran muy bajos y, por lo tanto, aportaban muy poco valor nutricional durante la etapa de crecimiento de las plantas.
Otro tratamiento fue la aplicación del microorganismo Azospirillum brasilense, comercialmente conocido como DIMAZOS, proveniente de Biocultivos, con una concentración de 1×10⁸ UFC/ml (Comercial Proveedor et al., 2019).
Tratamientos
Con base en los tratamientos mencionados, el diseño experimental incluyó tres tratamientos y un control, cada uno con una cama: Azospirillum brasilense (TA), Biol (TB), Biol + Azospirillum brasilense (TBA), Control (C): adición de agua sin microorganismos ni biol.
El tratamiento TA consistió en 5 ml por planta, aplicado una sola vez durante la siembra de las plántulas. El tratamiento TB fue de 50 ml por planta. Finalmente, el tratamiento TAB consistió en 5 ml de Azospirillum brasilense inicial y 50 ml de biol, aplicados semanalmente.
Las plantas se regaron cuatro veces por semana, aplicando 500 ml de agua en la parte superior de cada cama en cada riego.
Desde la semana 1, se evaluaron variables biométricas como altura (cm), diámetro del tallo (mm) y número de hojas. Luego, las plantas fueron recolectadas para pesarse en una balanza analítica, tanto la parte radicular como la foliar, con el fin de obtener biomasa fresca. Estas muestras se colocaron en un horno a 60°C durante 3 días para obtener la biomasa seca.
Para el análisis foliar, se enviaron muestras a un laboratorio para medir el porcentaje de macro y micronutrientes mediante espectrofotometría de absorción atómica.
Para verificar la colonización de Azospirillum brasilense, su presencia o ausencia en la rizosfera se comprobará verificando su crecimiento continuo mediante un cultivo de bacterias oxidantes de amonio (AOB). Estos análisis seguirán el protocolo establecido por el Instituto Geográfico Agustín Codazzi.
Resultados y análisis de la etapa de ajuste
Es el producto final obtenido de un proceso de estabilización de efluentes, en el cual intervienen una serie de operaciones unitarias que controlan el entorno y mantienen una acción bacteriana estable, haciendo del biol Terrazonet un producto estabilizado de excelente calidad.
El efluente es un sustrato orgánico líquido obtenido de la descomposición anaeróbica (sin oxígeno) y térmica (con temperatura) de residuos orgánicos, mediante poblaciones de microorganismos presentes en los propios residuos y otros obtenidos de caldos microbianos de lodos anaerobios, bajo condiciones controladas (relación agua/residuo, pH, temperatura, tamaño de partícula, ausencia de aire, relación C/N).
Este proceso produce un material estable llamado biol, que al aplicarse al suelo ejerce una influencia favorable sobre sus propiedades físicas, químicas y biológicas.(A.J. Zapata, 2024) La Tabla 3 muestra los resultados obtenidos de la caracterización del biol comercial.
Análisis tabla 3
Tabla 3. Análisis fisicoquímico del digestato Terrazonet
| ANÁLISIS FÍSICO-QUÍMICO DEL BIOL TERRAZONET | |||||
| PARÁMETRO | TÉCNICA | NORMA | RESULTADO | D.E. | UNIDAD |
| Calcio total | E.C | No aplica | 0.48 | 0.01 | g/L |
| Magnesio total | E.C | No aplica | 0.0871 | 0.0001 | g/L |
| Níquel total | A.A | SM3111B | 1.12 | 0.03 | ppm |
| Potasio total | E.C | No aplica | 0.83 | 0.01 | g/L |
| Sodio total | E.C | No aplica | 0.317 | 0.001 | g/L |
| Zinc total | E.C | No aplica | 0.00398 | 0.00005 | g/L |
| Carbono orgánico oxidable | Titulométrica | NTC 5167 | 1.59 | – | % |
| Conductividad eléctrica (1/200) | Potenciometría | NTC 5167 | 0.95 | – | dS/m |
| Densidad (20 °C) | Gravimetría | NTC 5167 | 1 | – | g/cm³ |
| Fósforo total | Espectrofotometría | NTC 234 | 0.45 | – | % |
| Sólidos suspendidos totales | Gravimetría | SM 2540D | 673 | – | mg/L |
| Nitrógeno orgánico total | Kjeldahl | NTC 370 | 1.13 | – | % |
| pH (10%) | Potenciometría | NTC 5167 | 7.15 | – | – |
| Relación C/N | No aplica | No aplica | 1.4 | – | – |
En la Tabla 3, se muestran los resultados de la caracterización del biol, los cuales se relacionan con la NTC 5167 de 2022, destacando parámetros importantes como el pH, que indica el nivel de acidez presente en la muestra. El resultado fue un pH de 7.15, ideal para la presencia de macronutrientes y micronutrientes esenciales para el crecimiento y desarrollo de las plantas, así como para sus funciones metabólicas o estructurales (Zainuddin et al., 2022).
Los nutrientes proporcionados por el biol incluyen calcio, esencial para el desarrollo de las paredes celulares; magnesio, componente fundamental de la clorofila involucrado en la fotosíntesis; níquel, que en pequeñas cantidades ayuda en la actividad enzimática y metabólica; potasio, que regula el agua, la síntesis de proteínas y la resistencia a enfermedades; sodio, que debe mantenerse bajo para evitar toxicidad; y zinc, esencial para el crecimiento. Todos estos nutrientes se encuentran dentro de los rangos ideales para el cultivo de maíz. (A.J. Zapata, 2024)
Resultados de contenido
El contenido de carbono orgánico es bajo en los fertilizantes líquidos (1.59%), lo cual puede variar según el efluente. Con este porcentaje de carbono orgánico oxidable, se busca aumentar la capacidad de retención de agua, estimular la actividad microbiana y, a su vez, incrementar la disponibilidad de nutrientes y mejorar la estructura del suelo.
La conductividad eléctrica garantiza la etapa de crecimiento del maíz, y el biol debe encontrarse entre 0.5 y 2.5 dS/m, asegurando que el fertilizante líquido tenga concentraciones de sales solubles suficientes para aportar los nutrientes necesarios sin causar estrés salino a las plantas.
El fósforo presente en el biol favorece el desarrollo radicular y la floración. En este caso, tiene una concentración de 0.45%, dentro del rango ideal de 0.5% a 5%.
Los fertilizantes líquidos nitrogenados están diseñados para suministrar este nutriente en una forma fácilmente disponible para las plantas, con un rango de 1% a 10%. El biol suministrado aporta 1.13%.
Los análisis microbianos del digestato comercial muestran concentraciones de (UFC/g): mesófilos 3,3 × 10⁵, termófilos 8,0 × 10², mohos 2,4 × 10², levaduras 8,70 × 10², enterobacterias 5,00 × 10¹, mientras que nematodos y/o protozoos están ausentes y resultó negativo para Salmonella, lo que lo hace adecuado para su aplicación en diferentes tratamientos.
Gráfico
La Figura 3 (a) presenta los resultados de la altura de las plantas medida durante las 14 semanas de ensayo. Se observa un incremento discontinuo en la altura de la biomasa aérea, con diversas variaciones y comportamientos entre los tratamientos.
De la semana 2 a la 4, se observaron los comportamientos esperados: el tratamiento Biol + Azospirillum mostró un avance significativo respecto a los demás, mientras que el control presentó el menor crecimiento.
Durante las semanas 5, 6 y 7, los tratamientos control y Azospirillum exhibieron mayores aumentos de altura aérea que los otros tratamientos. En las semanas 13 y 14, se observó el mayor crecimiento en todos los tratamientos excepto en el control.
Análisis de resultados del gráfico
Figura 3 (b) presenta los resultados del número promedio de hojas por tratamiento, medidos durante las 14 semanas del ensayo. Se observa una tendencia de crecimiento lineal hasta la semana 5, lo que indica la formación de nuevas hojas por planta sin pérdida hasta ese punto, siendo el tratamiento con Biol + Azospirillum el que presentó el mayor número de hojas. Desde la semana 6 hasta la semana 14, el tratamiento control experimentó una pérdida significativa de hojas, con la muerte de dos plantas de este grupo: una en la semana 6 y otra en la semana 7.
Los tratamientos con menor pérdida foliar fueron el tratamiento con Biol y el tratamiento con Azospirillum. Esto se debe a que el tratamiento Biol + Azospirillum presentó una mayor pérdida de hojas en la semana 7 debido a una invasión de insectos en esa cama. Se llevó a cabo un proceso de fumigación que permitió la recuperación de las plantas desde la semana 8 hasta la semana 14, mostrando resultados satisfactorios en el ensayo.
Etapa R2
En esta etapa de ajuste, las plántulas de maíz alcanzan la etapa R2, también conocida como la etapa de ampolla, donde los granos se llenan con un líquido transparente y se puede ver el embrión en la mayoría de las plántulas de maíz. Esta etapa comprende 4 subetapas adicionales en comparación con la primera etapa exploratoria del ensayo: Vn, donde se hace visible el cuello de la “n”‑ésima hoja (“n” corresponde al número final de hojas que tiene la planta; generalmente varía entre 16 y 22, pero para el momento de la floración se habrán perdido las 4 a 5 hojas inferiores); etapa VT, donde la última rama de la panoja es completamente visible; etapa R0, también conocida como antesis o floración masculina, donde comienza a liberarse el polen; y etapa R1, donde los estigmas son visibles.
Etapa de desmonte
Después de la semana 14 inicia el proceso experimental de desmontaje, donde se mide la altura de la planta y se toma el peso fresco de la biomasa tanto de la parte aérea como del sistema radicular. Las plantas se exponen al sol durante una semana para el proceso de secado y pérdida de humedad. Tras este periodo, se registra el peso seco de la biomasa, tanto foliar como radicular.

Fig 4. (a) Biomasa aérea fresca de las plantas de Zea mays durante la fase de ajuste a lo largo de 14 semanas. (b) Biomasa radicular fresca de las plantas de Zea mays durante la fase de ajuste a lo largo de 14 semanas. Fuente: (V. Jaramillo & A. Zapata, 2024)
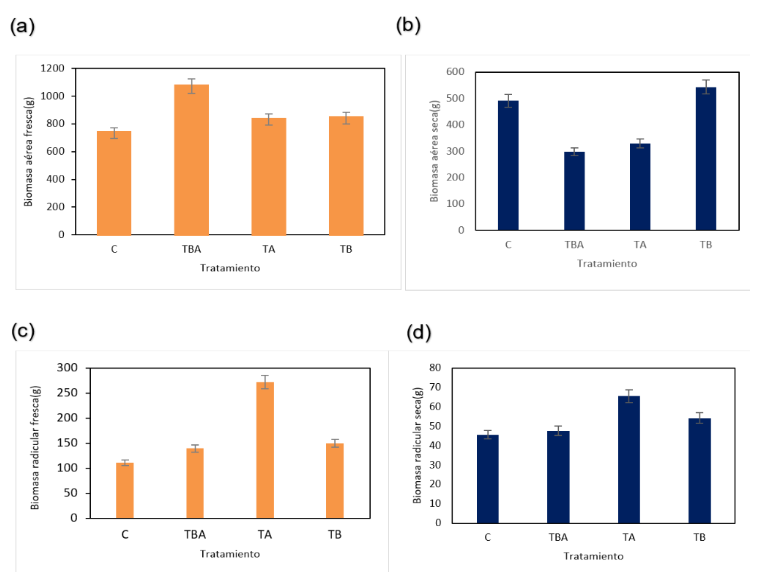
Fig 5. (a) Biomasa aérea fresca de las plantas de Zea mays durante la fase de ajuste a lo largo de 14 semanas. (b) Biomasa aérea seca de las plantas de Zea mays durante la fase de ajuste a lo largo de 14 semanas. (c) Biomasa radicular fresca de las plantas de Zea mays durante la fase de ajuste a lo largo de 14 semanas. (d) Biomasa radicular seca de las plantas de Zea mays durante la fase de ajuste a lo largo de 14 semanas. Fuente: (V. Jaramillo & A. Zapata, 2024)
Figura 4 (a)
Según los datos de la Figura 4 (a), la biomasa aérea fresca de las plantas de maíz que recibieron el tratamiento con Azospirillum + Biol sugiere que las plantas se encontraban saludables y en buenas condiciones de crecimiento, con adecuada disponibilidad de luz, agua y nutrientes. En este tratamiento se puede inferir que el riego, la fertilización y el control de plagas contribuyeron a su desarrollo. Considerando que su biomasa aérea fresca superó los 1000 g, puede correlacionarse con un mejor rendimiento de cosecha.(A.J. Zapata, 2024) El tratamiento con Azospirillum + Biol arrojó resultados más favorables que los otros dos tratamientos y el control. Sin embargo, cabe destacar que los tratamientos individuales con Azospirillum y Biol presentaron biomasa aérea fresca entre 800 y 900 g, mientras que el control estuvo por debajo de 800 g.
Figura 4 (b)
De acuerdo con la Figura 4 (b), los datos de biomasa aérea seca después del proceso de secado para los tratamientos con Azospirillum y Azospirillum + Biol indican un rendimiento moderado. Este resultado puede considerarse suficiente o insuficiente, ya que refleja limitaciones en el proceso de fotosíntesis, el cual influye tanto en la calidad como en la cantidad de la cosecha, siendo un factor crucial para la planificación agrícola. En el caso del tratamiento con Biol y el control, los datos de biomasa aérea seca representan el potencial de rendimiento de la planta, ya que una mayor biomasa aérea seca se asocia con una mayor producción de grano. (A.J. Zapata, 2024) Esto también sugiere que las plantas tuvieron buenas condiciones de crecimiento en términos de luz, agua y nutrientes. El tratamiento con Biol destacó con 543,87 gramos, superando los demás tratamientos y el control.
Figura 4 (c)
Según los datos de la Figura 4 (c), la biomasa radicular fresca de las plantas de maíz que recibieron el tratamiento con Azospirillum indica que la masa radicular es considerablemente saludable. Una mayor biomasa radicular significa que la planta tiene un sistema de raíces bien desarrollado, lo que favorece la absorción eficiente de nutrientes y agua del suelo. Este sistema radicular robusto permite a la planta resistir condiciones adversas, como suelos secos o con baja disponibilidad de nutrientes. Además, esta biomasa radicular contribuye a mejorar la estructura del suelo y la actividad microbiana, lo cual beneficia directamente a la planta. El tratamiento con Azospirillum presentó resultados mucho más favorables que los otros tratamientos y el control, con un total de 271,955 g de biomasa radicular fresca.
Figura 4 (d)
Según los datos de la Figura 4 (d), la biomasa radicular seca de las plantas de maíz tratadas con Azospirillum indica que la masa radicular es considerablemente saludable. Una mayor biomasa radicular implica un sistema radicular bien desarrollado, lo que permite una absorción más eficiente de agua y nutrientes del suelo. Este sistema radicular desarrollado ayuda a la planta a resistir condiciones adversas, como sequías o suelos pobres en nutrientes. Asimismo, contribuye a mejorar la estructura del suelo y la actividad microbiana, beneficiando el desarrollo general de la planta. El tratamiento con Azospirillum mostró resultados mucho más favorables que los otros tratamientos y el control, con un total de 65,5 g de biomasa radicular seca.
Relevancia para la vida diaria y decisiones ciudadanas de los biofertilizantes
La información presentada en este estudio no sólo es relevante para el sector agrícola, sino también para cualquier ciudadano, ya que el uso de biofertilizantes y abonos líquidos como los bioles impacta directamente la calidad de los alimentos que consumimos y la salud del suelo del que dependemos. Comprender cómo microorganismos como Azospirillum brasilense mejoran el crecimiento de las plantas permite a las personas identificar prácticas más sostenibles para sus propios cultivos en huertas caseras, jardines o proyectos comunitarios. Además, este conocimiento brinda herramientas para tomar decisiones informadas al apoyar productos agrícolas cultivados con métodos más limpios, reduciendo la dependencia de químicos sintéticos y contribuyendo a un ambiente más saludable. En la vida diaria, estos principios pueden aplicarse eligiendo fertilizantes naturales, promoviendo la separación de residuos orgánicos para la producción de abonos líquidos y participando en iniciativas de agricultura urbana que fortalecen la seguridad alimentaria local.
Conclusiones
Durante las etapas de desarrollo de la investigación, el suelo presentó una textura franco arcillosa arenosa y un pH de 5,5. Esto permitió demostrar que las plantas de maíz son tolerantes a un pH ligeramente ácido durante su etapa de crecimiento.
En la etapa exploratoria se evidenció que la baja disponibilidad de área de sustrato generó un déficit nutricional en las plantas, afectando la tasa de absorción y translocación de nutrientes. Esto se corrigió en la fase de ajuste, donde se obtuvo un desarrollo del sistema radicular altamente ramificado en cada uno de los tratamientos, lo que permitió la adaptabilidad a las condiciones ambientales del lugar.
De los tratamientos analizados, los que destacaron en el análisis de biomasa fresca fueron las rizobacterias y la combinación de estas con biol orgánico. Por tanto, se infiere que la aplicación de estos tratamientos a gran escala es viable para cultivos de maíz, funcionando como un estímulo y preparación de los mismos ante períodos de estrés hídrico. Además, se cumplen las buenas prácticas agrícolas y los Objetivos de Desarrollo Sostenible (ODS).
Referencias
- CIBIOGEM. (2003). Consensus document on the biology of Zea mays subsp. mays.
- Comercial Proveedor, N., Fabricante, /, & Dirección, F. (2019). Dimazos 100 SC. www.biocultivos.com.co
- Haiyang, L. (2022). Liquid organic fertilizer amendment alters rhizosphere microbial community: EBSCOhost. https://web.p.ebscohost.com/ehost/pdfviewer/pdfviewer?vid=16&sid=c587fecd-1cbb-45fc-b6a5-f2f5ca20f86e%40redis
- Icontec. (2022). NTC 5167. Productos para la industria agrícola: Productos orgánicos usados como abono o fertilizantes y enmiendas o acondicionadores de suelo.
- Instituto de la Potasa y el Fósforo. (2015). Conozca y resuelva los problemas del maíz.
- Lanfranco, J. W., Pellegrini, A. E., & Cattani, V. M. (2014). Contenido de edafología: Génesis y evolución de propiedades fisicoquímicas del suelo (pp. 164–165). Universidad de La Plata. https://elibro.net/es/ereader/colmayor/66430?fs_q=propiedades__quimicas__del__suelo&prev=fs
- Levin, K. S., Auerswald, K., Reents, H. J., & Hülsbergen, K. J. (2021). Effects of organic energy crop rotations and fertilisation with the liquid digestate phase on organic carbon in the topsoil. Agronomy, 11(7). https://doi.org/10.3390/agronomy11071393
- Makádi, M., Szegi, T., Tomócsik, A., Orosz, V., Michéli, E., Ferenczy, A., Posta, K., & Biró, B. (2016). Impact of digestate application on chemical and microbiological properties of two different textured soils. Communications in Soil Science and Plant Analysis, 47(2), 167–178. https://doi.org/10.1080/00103624.2015.1109652
- Marín García, M. L. (2003). Análisis químico de suelos y aguas (p. 105). Universidad Politécnica de Valencia.
- Naciones Unidas. (n.d.). The Sustainable Development Goals Report 2023 (Spanish edition).
- Rai, P. K., Rai, A., Sharma, N. K., Singh, T., & Kumar, Y. (2023). Limitations of biofertilizers and their revitalization through nanotechnology. Journal of Cleaner Production, 418. Elsevier Ltd. https://doi.org/10.1016/j.jclepro.2023.138194
- Sharma, P., Bano, A., Verma, K., Yadav, M., Varjani, S., Singh, S. P., & Tong, Y. W. (2023). Food waste digestate as biofertilizer and their direct applications in agriculture. Bioresource Technology Reports, 23, 101515. https://doi.org/10.1016/j.biteb.2023.101515
Investigaciones
- Allouzi, S. M. A., Keng, Z. X., Supramaniam, C. V., Singh, A., & Chong, S. (2022a). Liquid biofertilizers as a sustainable solution for agriculture. Heliyon, 8(12). Elsevier Ltd. https://doi.org/10.1016/j.heliyon.2022.e12609
- Garbanzo-León, G., Alemán-Montes, B., Alvarado-Hernández, A., & Henríquez-Henríquez, C. (2017). Validación de modelos geoestadísticos y convencionales en la determinación de la variación espacial de la fertilidad de suelos del Pacífico Sur de Costa Rica. Investigaciones Geográficas, 2017(93), 20–41. https://doi.org/10.14350/rig.54706
- Angulo-Castro, A., Ferrera-Cerrato, R., Alarcón, A., Almaraz-Suárez, J. J., Delgadillo-Martínez, J., Jiménez-Fernández, M., & García-Barradas, O. (2018). Growth and photochemical efficiency of photosystem II in seedlings of two varieties of Capsicum annuum L. inoculated with rhizobacteria and arbuscular mycorrhizal fungi. Revista Argentina de Microbiología, 50(2), 178–188. https://doi.org/10.1016/j.ram.2017.03.011
- Atieno, M., Herrmann, L., Nguyen, H. T., Phan, H. T., Nguyen, N. K., Srean, P., Than, M. M., Zhiyong, R., Tittabutr, P., Shutsrirung, A., Bräu, L., & Lesueur, D. (2020). Assessment of biofertilizer use for sustainable agriculture in the Great Mekong Region. Journal of Environmental Management, 275. Academic Press. https://doi.org/10.1016/j.jenvman.2020.111300
- CGIAR. (n.d.). Consorcio mundial de investigación para un futuro sin hambre: Alliance Bioversity y CIAT.
- Chen, J., Zhang, J., Ma, D., & Zhang, C. (2019). Organic amendment mitigates the negative impacts of mineral fertilization on bacterial communities in Shajiang black soil. https://doi.org/10.1016/j.apsoil.2019.103457
- Chin Cheong, J., Lee, J. T. E., Wei Lim, J., Song, S., Tan, J. K., Yu Chiam, Z., Yee Yap, K., Yang Lim, E., Zhang, J., Tan, H. T., & Wah Tong, Y. (2020). Closing the food waste loop: Food waste anaerobic digestate as fertilizer for the cultivation of the leafy vegetable, xiao bai cai (Brassica rapa). https://doi.org/10.1016/j.scitotenv.2020.136789
- Chuda, A., & Ziemiński, K. (2023). Ultrafiltration of digestate liquid fraction by hollow-fiber membranes: Influence of digestate pre-treatment on hydraulic capacity and nutrient removal efficiency. Chemical Engineering Journal, 473. https://doi.org/10.1016/j.cej.2023.145426
Ficha técnica
- Autor: Verónica Jaramillo Saldarriaga
- Fecha de elaboración: 16/11/2024
- Fecha de publicación: 30/01/2026
- Categoría para la web: Investigaciones






